
市場概要
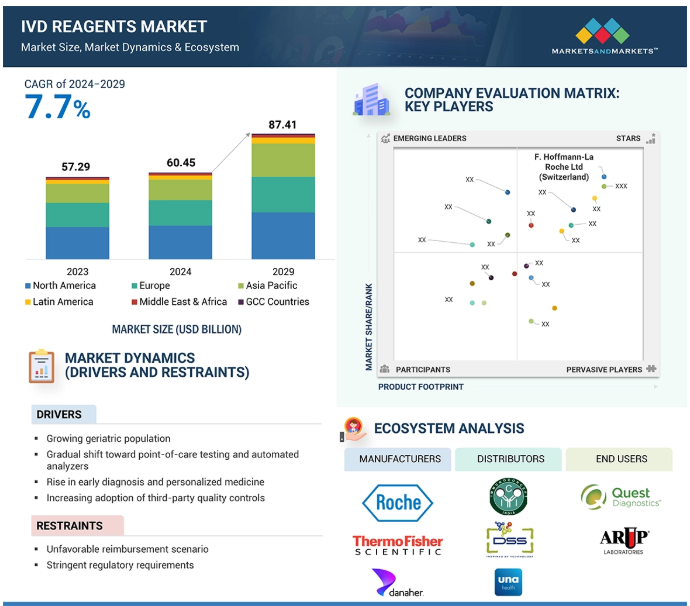
世界のIVD試薬市場は、2023年に5,729万米ドルでしたが、年平均成長率は7.7%と堅調に推移し、2024年には6,045万米ドル、2029年には8,741万米ドルに達すると予測されています。体外診断用医薬品試薬市場の成長は、主に診断精度の向上に焦点を当てた分子診断学の技術革新が牽引しています。早期発見のための予防医療に対する意識の高まりも市場の成長に寄与しています。慢性疾患の増加も市場成長を促進する重要な要因です。
従来の検査室以外で実施される検査は、患者により近い場所でケアを提供したいという需要の高まりにより、今後数年間で増加する見込みです。ポイント・オブ・ケア(POC)検査試薬を通じて利用できる検査の種類は、近年大幅に拡大しています。例えば、イムノアッセイベースのPOC検査分析装置は、患者のコンプライアンスを確保しながら高い感度を提供します。さらに、これらのシステムは、HIV、マラリア、デング熱、結核、C型肝炎などの様々な疾患の診断と管理に必要な時間を短縮するのに役立ちます。
米国や欧州諸国では、体外診断用医薬品(感染症診断薬を含む)に適用される規制や法的要件が厳しくなっています。米国では IVD 製品は 21 CFR 809 で定義され、医療用試薬と同様のガイドラインに基づいて規制されています。FDAは新しいFDAガイダンス文書を発表しました。米国連邦規制では、機器メーカーは機器のさらなる変更について510(k)申請書を提出しなければなりません。新しい申請では、ソフトウェアの更新や既存の機器へのインストール、またはこれらの試薬に加えられるその他の変更が必要になる場合があります。
EUは、指令98/79/ECおよびそれ以前のいくつかの指令から体外診断用医薬品規則(IVDR)(規則(EU)2017/746)に移行し、新しい規制の枠組みに従ってEUで合法的に販売するためには、製品に(Conformité Européenne)CEマークを付ける必要があります。IVDRには2022年5月26日に終了する移行期間があり、2017年5月26日に施行されました。一部の体外診断用医薬品の承認に必要な期間は不確定であり、規制当局が承認を拒否した場合、研究開発への投資が無駄になる可能性があります。
コンパニオン診断薬には、医療従事者が治療に対する最適な反応に基づいて患者の治療方針を決定するのを支援することを目的とした検査やアッセイが含まれます。コンパニオン診断薬を治療薬と共同開発することで、医薬品開発プロセスを大きく変えることができ、治療効果を高めたより安全な医薬品を迅速かつコスト効率よく得ることで、医薬品候補を商業化することができます。高価格の専門治療薬やより安全性の高い薬剤に対する需要の増加に伴い、コンパニオン診断薬市場は高い成長の可能性を秘めています。コンパニオン診断薬の重要性の高まりは、診断薬部門、ひいては体外診断用医薬品市場にも成長機会をもたらします。
微生物の急速な変異や伝染病の増加により、臨床検査室は迅速なサンプル診断が可能な革新的技術を導入する必要があります。しかし、高度な診断製品を操作できる熟練した検査技師の不足が、特に新興市場における全体的な採用の妨げとなっています。さらに、手作業から自動化への移行に対する消極的な姿勢も、市場成長の課題となっています。多くの医療機関は、手作業や従来型のアプローチからITベースのアプローチへの移行が難しいと感じているか、移行を好まない可能性があります。
エコシステム分析は、IVD試薬市場に存在する要素を描写し、特定の市場の相互関連する構成要素を理解することで、市場に徹底的に影響を与えます。IVD試薬の利害関係者は、エンドユーザーやアプリケーションなどの重点分野で構成されます。IVD試薬市場は、試薬の種類、アプリケーション、技術、検査タイプ、エンドユーザーの4つのセグメントに分けられます。
主要企業・市場シェア
種類別では、抗体、抗原、精製タンパク質・ペプチド、オリゴヌクレオチド、核酸プローブ、その他のIVD試薬に分類されます。抗体は、特に自己免疫疾患や腫瘍学など、臨床現場において幅広い用途があります。抗体を提供する主要企業には、BD(米国)、Revvity(米国)、Grifols, S.A.(スペイン)などがあります。体外診断用医薬品市場における抗体の高いシェアは、テーラーメイド診断における精度の向上と高感度化によるものです。
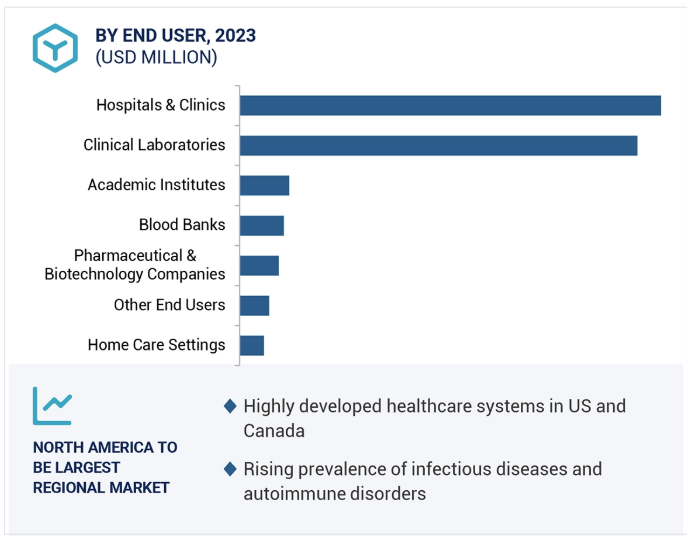
体外診断用医薬品市場は、エンドユーザー別に病院・診療所、臨床検査室、血液バンク、在宅医療、製薬・バイオテクノロジー企業、学術機関、その他のエンドユーザーに分類されます。臨床検査室は、病気とその治療を特定・検出するための診断検査を行っています。高い市場成長は、感染症、血液学、臨床化学、免疫学、病理学の診断検査数が増加しているためです。
体外診断用医薬品の世界市場は6つの主要地域に区分されます: 北米、ヨーロッパ、アジア太平洋地域、中東・アフリカ、中南米、GCC諸国。2023年、IVD試薬市場の最大セグメントは北米。この地域には主要なIVD試薬メーカーが存在することが市場成長を促進する主な要因です。体外診断用医薬品の償還シナリオも複雑ではありません。また、この地域における疾病の有病率の増加も、米国とカナダにおける体外診断用試薬市場の成長を促進すると期待されています。
2024年9月、Thermo Fisher Scientific Inc.(米国)は、世界中の製薬開発向けに高度なラボサービスと機器を提供する検査/ラボセンターを導入しました。
2023年12月、Danaher Corporation(米国)がAbcam(英国)を買収し、創薬、ライフサイエンス研究、診断の進歩に不可欠なバイオ分野を拡大。
2023年12月、F. Hoffmann-La Roche Ltd(スイス)がLumiraDx(米国)のポイントオブケア技術を買収する最終契約を締結。
2022年5月、Hologic, Inc.(米国)はPanther Fusion EBV Quant AssayとPanther Fusion BKV Quant Assayの2つの新しい分子アッセイのCEマーキングを取得し、Panther Fusionシステムでの移植病原体モニタリングメニューを拡大。
IVD試薬市場の主要企業は以下の通り。
Danaher Corporation (US)
F. Hoffmann-La Roche Ltd (Switzerland)
Abbott (US)
Siemens Healthineers AG (Germany)
Thermo Fisher Scientific Inc. (US)
Illumina, Inc. (US)
BioMerieux (France)
BD (US)
Hologic, Inc. (US)
Bio-Rad Laboratories, Inc. (US)
Sysmex Corporation (Japan)
QIAGEN N.V. (Netherlands)
Agilent Technologies, Inc. (US)
Revvity (US)
DiaSorin S.p.A (Italy)
Grifols, S.A. (Spain)
Werfen, S.A. (Spain)
QuidelOrtho Corporation (US)
Chembio Diagnostics, Inc. (US)
Surmodics, Inc. (US)
Merck KGaA (Germany)
MEDICAL & BIOLOGICAL LABORATORIES CO., LTD. (Tokyo)
Canvax (Spain)
Prestige Diagnostics (US)
Adaltis S.r.l. (Italy)
【目次】
はじめに
研究方法論
要旨
プレミアムインサイト
市場概要
5.1 はじめに
5. 2 市場ダイナミクス DRIVERS●高齢者人口の増加●ポイントオブケア検査と自動分析機への漸進的シフト●早期診断と個別化医療の台頭●第三者品質管理の採用の増加●バイオテクノロジーとバイオ医薬品産業の成長●研究開発活動への資金拠出の増加 RESTRAINTS●償還シナリオの不利●規制要件の厳しさ 不利な償還シナリオ- 厳しい規制要件- 事業機会- バイオマーカー開発の増加- コンパニオン診断薬の重要性の高まり- 新興国における市場成長機会- デジタル化のトレンドの高まり 事業課題- 臨床プロセスにおける運用上の課題
5.3 顧客のビジネスに影響を与えるトレンド/混乱
5.4 価格分析 主要企業の平均販売価格動向(アプリケーション別 主要企業の平均販売価格動向(地域別 平均販売価格動向(技術別
5.5 バリューチェーン分析
5.6 サプライチェーン分析
5.7 エコシステム分析
5.8 投資と資金調達のシナリオ
5.9 技術分析 主要技術 副次的技術- 多重ポイントオブケア検査- 核酸ラテラルフロー免疫測定- DNAベースの検出- 免疫診断学- デュアルパス技術
5.10 特許分析
5.11 貿易分析 輸入データ 輸出データ
5.12 主要会議とイベント(2024-2025年
5.13 ポーターの5つの力分析 新規参入の脅威 代替品の脅威 供給者の交渉力 買い手の交渉力 競争相手の強さ
5.14 規制情勢分析 北米、ヨーロッパ、アジア太平洋地域、中南米、中東 規制機関、政府機関、その他の組織 北米、ヨーロッパ、アジア太平洋地域、中南米、中東・アフリカ、GCC諸国
5.15 主要ステークホルダーと購買基準 購買プロセスにおける主要ステークホルダー 購買基準
5.16 AI/ジェネレーティブAIのIVD試薬市場への影響 IVD試薬の市場の可能性 AIのユースケース AIを導入している主要企業 IVD試薬におけるジェネレーティブAIの将来性
IVD試薬市場、種類別
6.1 はじめに
6.2 抗ヒスタミン抗体 モノクローナル抗体- 癌の罹患率の増加が成長を刺激 ポリクローナル抗体- 感染症や自己免疫疾患の有病率の増加が成長をサポート
6.3 抗原、精製タンパク質、ペプチド 先進的な精密医療への関心の高まりが成長を促進
6.4 オリゴヌクレオチド-分子診断への志向の高まりが市場を牽引
6.5 疾患の早期発見と低存在バイオマーカーのモニタリングに対する核酸プロー ブのニーズが成長を後押し
6.6 その他のIVD試薬
IVD試薬市場、技術別
7.1 導入
7.2 自動化傾向の高まりが成長を促進する免疫測定法
7.3 糖尿病罹患率の上昇がセグメントを押し上げる臨床化学
7.4 血液スクリーニングとポイントオブケア検査の需要拡大が市場を後押し
7.5 幹細胞研究への関心の高まりが血液学の成長を加速
7.6 微生物学 微生物感染症の蔓延が市場を活性化
7.7 抗凝固療法の普及が市場を牽引する凝固・止血領域
7.8 尿検査 腎臓病の有病率の上昇が市場成長を後押し
7.9 疾患スクリーニング、法医学分析、薬物治療におけるアプリケーションの増加 が市場を後押しするクロマトグラフィー&質量分析
7.10 免疫組織化学 癌診断のための臨床検査件数の増加が市場を牽引
IVD試薬市場、用途別
8.1 導入
8.2 製品の上市と承認が増加する感染症が市場を牽引
8.3 早期診断と質の高い治療が重視される腫瘍学的用途が市場を活性化
8.4 内分泌学的アプリケーション 糖尿病と甲状腺関連疾患の有病率の上昇が成長を維持
8.5 先進国および発展途上国におけるライフスタイルの変化が市場を促進する循環器系アプリケーション
8.6 自動診断機器の採用が増加する血液スクリーニングが成長を促進
8.7 希少疾患や致死的疾患の診断に遺伝子検査の採用が増加し、成長を維持
8.8 自己免疫疾患検査技術、試薬、代替アッセイ法の進歩が市場を牽引
8.9 アレルギー診断:アレルギー治療と予防への関心の高まりが成長を加速
8.10 薬物モニタリング・検査:乱用薬物検査の実施拡大が市場を牽引
8.11 その他の用途
IVD試薬市場:検査種類別
9.1 導入
9.2 自動化の必要性が高まるラボ検査が成長を促進
9.3 患者の状態を綿密にモニタリングする必要があるポイントオブケア検査が成長を促進
IVD試薬市場:エンドユーザー別
10.1 導入
10.2 病院・診療所では専門的な診断検査が増加し、成長を加速
10.3 臨床検査機関 大規模なリファレンス・ラボラトリー – 専門的な検査能力と最短の納期へのニーズが市場を押し上げる 中小規模のラボラトリー – 自動化・半自動化機器の採用が成長を後押し
10.4 血液バンク:外傷症例の増加と高度な外科手術の可能性が市場を後押し
10.5 在宅医療現場における在宅検査キットへの嗜好の高まりが市場を牽引
10.6 製薬・バイオテクノロジー企業の研究開発努力の増大が成長に寄与
10.7 産学連携を進める学術機関が成長を後押し
10.8 その他のエンドユーザー
…
【本レポートのお問い合わせ先】
www.marketreport.jp/contact
レポートコード:MD 9227