
市場概要
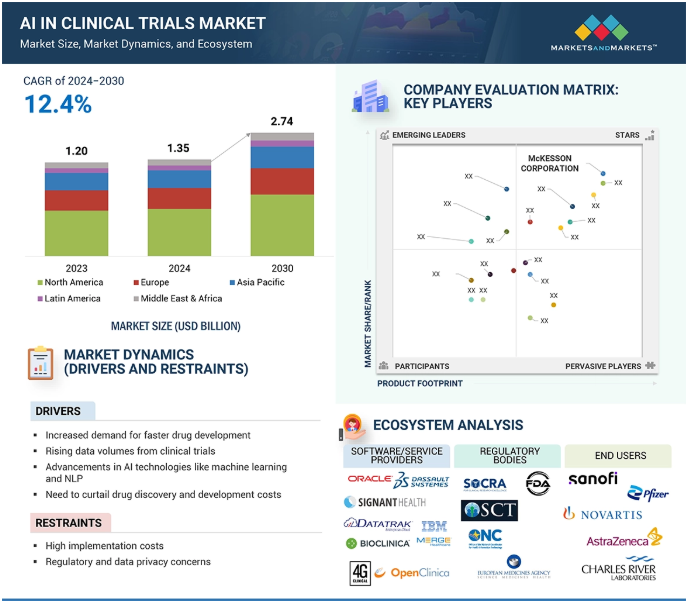
臨床試験AIの世界市場規模は2023年に12億米ドルでしたが、年平均成長率は12.4%と堅調に推移し、2024年には13億5,000万米ドル、2030年には27億4,000万米ドルに達すると予測されています。臨床試験におけるAI市場は、患者中心かつ患者主導型の臨床試験に対する需要の高まりに牽引され、大きな成長を遂げています。また、個別化治療の傾向の高まりも、治療の方向付けのためのDNA情報の精査を容易にするため、医療における人工知能の成長の一因となっています。さらに、研究関連データの管理におけるAIのニーズや、プロセスの設計や精度の高い意思決定のための研究データは、成長にプラスの影響を与えています。さらに、臨床データの精巧な性質が高まり、試験目的のためのその処理は、膨大な量のデータを処理し、試験進捗のための洞察を提供するAIの高度な分析に依存しています。
臨床試験は医薬品開発のバックボーンであり、製薬企業やバイオテクノロジー企業が新製品を上市するのに役立ちます。過去10年間、世界的に臨床試験の需要は急増し、現在の医療ニーズに従って、新しい治療薬を開発する必要性も急増しています。ClinicalTrials.govによると、2023年8月現在、世界中で約461,614件の臨床試験が記録されており、2000年の5,475件から大幅に増加しています。
世界市場における臨床試験の増加は、その地域における臨床試験を刺激し、市場の成長につながります。2022年12月の世界保健機関(WHO)の臨床試験登録によると、最も多くの臨床試験が北米とヨーロッパで実施されています。実施された臨床試験の数は、米国が〜23%で最も多く、次いで中国、日本、インド、ドイツとなっています。米国の製薬・バイオテクノロジー産業が非常に確立されていることも、研究開発費の継続的な増加やCROSの数の多さとともに、この分野での競争をリードする成功の要因となっています。
CROSは、製薬・バイオテクノロジー企業や学術・研究機関と同様のサービスを有資格で経験豊富な科学者に提供しているため、高度なスキルを持つ専門家を惹きつけ、維持する難しさに直面しています。このような側面は、主に小規模の分析試験プロバイダーにとって、財務や結果に影響を与えがちな、より多くの報酬やその他のフリンジベネフィットを提供することを余儀なくされます。このような熟練した専門家の不足は、新しい技術や方法論の採用を妨げ、今後数年間の臨床試験市場の成長を抑制する可能性があります。グローバル・ワークフォース・インテリジェンス(GWI)プロジェクトによると、2025年までに210万人という天文学的な医療従事者の需給ギャップが生じ、3人に1人が未充足のまま職務を終えることになります。キャリアビルダーによると、2022年9月の統計では、米国で採用可能な人材はわずか570万人で、臨床研究職は660万人。さらに、1人のCRCが求職するのに7つのポジションがリストアップされています。Association of Clinical Research Organizationsによると、特に臨床試験アソシエイト(CTA)と臨床研究アソシエイト(CRA)の分野で深刻な不足が指摘されています。この10年来の危機は、製薬会社やCROによる新卒者のトレーニングが、業界からの研究要件を満たすスキルとして適切でないために深刻化しています。
従来、製薬企業、バイオテクノロジー企業、医療機器企業は、初期段階の開発プロジェクトや問題解決活動を社内で行い、主に後期段階の医薬品開発や定型的なプロセスをアウトソーシングしていました。しかし近年では、医薬品開発の初期段階で提携し、効率化を図る企業が増えています。
液体クロマトグラフィー質量分析計(LC/MS)、RNAシーケンス、遺伝子発現分析、コンペンディア原料の湿式化学分析、誘導結合質量分析計(ICP-MS)を用いた微量金属分析などの専門的な検査サービスを、原薬プロセス開発サイクルのかなり早い段階でアウトソーシングする企業が増えています。これらの専門的なサービスは、主に不純物の構造解明、溶媒除去(クラス I および II)、ハザード分析、カラムクロマトグラフィーの除去、全体的なコスト削減とプロセス効率向上の取り組みに使用されます。試験にはハイエンドの装置と訓練を受けた技術者が必要です。製薬会社やバイオテクノロジー企業は、設備や人件費を節約するために、専門的な試験サービスをCROSに委託したいと考えています。例えば、ファイザー、メルク、ロシュなどの企業は、研究開発パイプラインを充実させ、さまざまな治療分野における新薬化合物に対する需要の高まりに対応するため、社内試験サービスを縮小しています。
多くの製薬・バイオテクノロジー企業は、製品ポートフォリオを多様化し、新規の低分子・高分子を生み出すことに注力しています。企業は、未充足の要求に対応するため、併用療法、送達デバイス、改良または再設計された医薬品を開発しています。臨床研究部門は顧客と密接に連携しています。製品の複雑さを把握し、重要な臨床医薬品の提供を加速するための新しい創造的なソリューションを提案するための技術的な深みがあります。大企業が分析試験をアウトソーシングするその他の理由には、コスト削減、効率の向上、理想的な人材などがあります。このように、治療パイプラインがより複雑になるにつれ、製薬会社は、製品パイプラインに沿って化合物開発を加速させる新しい技術へのアクセスを得るために、CROSへのサービス委託を選択しています。
研究機関、CROS、パートナー企業、ソフトウェア企業の間でデータベースの数が増えるにつれ、データ漏洩の危険性が高まります。2009年の経済的および臨床的健康のための医療情報技術法(HITECH法)によると、対象となる事業体は、十分なプライバシー保護措置を講じることにより、個人の医療記録やその他の特定可能な医療情報を保護することが義務付けられています。その結果、エレクトロニクスツールを患者データベースに適用すると、患者記録のプライバシーに関する懸念が生じ、製薬企業が臨床試験ソフトウェアにAIを採用しながらプライバシーポリシーを遵守する上で、もう一つの大きな障壁となります。
臨床試験におけるAIのエコシステムは、テクノロジープロバイダー、製薬会社、CRO、規制当局、データプロバイダー、医療機関、患者支援団体などのプレーヤーで構成されています。メディデータのような技術プロバイダーは、データの分析と患者募集をそれぞれ支援するAIソフトウェアを開発し、IQVIAのようなCROは試験の実施にこれらのツールを導入しています。製薬企業やバイオテクノロジー企業もAIが医薬品開発プロセスをいかに最適化できるかを模索していますが、その成果は合法的かつ倫理的であることを確認するためにFDAなどの当局によって規制されています。フラットアイアン・ヘルスのようなデータ・プロバイダーは重要なデータセットを持ち、医療機関や大学は研究人材を提供しています。患者擁護団体は正義を推進し、差別に取り組むことで、生産的で成長志向の臨床AIイノベーション・エコシステムの存在を可能にしています。
臨床試験AI市場は機能別に、患者募集、試験デザイン最適化、データ管理・品質管理、有害事象予測・検出、薬剤再利用、規制遵守に区分されます。臨床試験におけるAI市場の機能別シェアでは、患者募集が最大を占めています。臨床研究を実施する上で最も大きな困難の1つは、有能な患者のリクルートと維持であり、約30%の臨床試験がリクルートの問題により失敗しています。AIが誘導するシステムは、EHR、SNS、遺伝子のデータベースなど数多くの要素を迅速にフィルタリングし、特定の試験に最適な個人を特定し、リクルートの精度とスピードを向上させる可能性があります。その結果、途中で募集スケジュールを大幅に修正することで、試験プロセス全体を合理化し、コストやリソースさえも削減することができます。さらに、AIがパーソナライズされたメッセージングや予測分析などのアプローチを通じて患者の治療プロセスへの参加を促進することで、脱落率が低下し、試験の成功確率が高まります。患者募集に特化したAIベースの開発に対する需要は、大手製薬企業でもマクロ主導の要因でも大きいため、患者募集が投資の重点となる可能性が高く、その結果、臨床試験におけるAIの市場シェアが高まることが説明できます。
臨床試験におけるAI市場は、用途に基づき、バイオマーカー、細胞・遺伝子治療、再生医療、医療機器・診断に区分されます。予測期間中に最も高い成長率を記録するのは細胞・遺伝子治療分野。これは、医療の個別化をさらに進めた分野の1つであり、治療が個人の遺伝的体質を考慮したものになることを意味し、患者に固有の多くのデータと洞察によって繁栄するものです。しかし、AIのような技術を利用することで、遺伝子データや臨床データの管理・分析が容易になり、臨床試験のデザインも改善され、患者の選択にも役立つため、細胞治療や遺伝子治療の進歩が促進されます。また、精密医療に対する規制当局の傾斜や、希少疾病を対象とした薬剤に対する膨大なニーズなど、いくつかの要因がこれらの臨床試験における人工知能への投資を促進しています。有効性、安全性、正確性の向上に関して、細胞・遺伝子治療に関する分かりやすい問題を管理するAIソリューションの貢献は、AIの採用によるこのセグメントの急成長を提唱するのに十分です。
主要企業・市場シェア
臨床試験におけるAI市場は、北米、ヨーロッパ、アジア太平洋地域、中南米、中東・アフリカに区分されます。2023年、臨床試験におけるAI市場で最も高いシェアを占めたのは北米です。北米が臨床試験におけるAI市場で最大のシェアを占めている背景には、数多くの要因があります。これには、同地域の高度な技術、医療研究開発への高額な支出、臨床研究を支援する既存の環境などが含まれます。米国の市場環境は、Pfizer社、Johnson & Johnson社、Amgen社など、医薬品合成、医薬品設計のターンアラウンド短縮、臨床試験のためのAIツール開発にリソースを投入している数多くの大手製薬企業やバイオテクノロジー企業によって特徴付けられています。また、北米はIBM、グーグル、マイクロソフトなどの企業がヘルスケアベースのAIシステムの開発に取り組んでおり、AI技術の震源地として認識されています。
同地域の効果的なヘルスケアフレームワークは、電子カルテ(EHR)の高度な普及と相まって、AIシステムが被験者の募集を支援したり、収集したデータの分析を行ったりすることを容易にします。さらに、食品医薬品局などの北米の規制当局は、これらのツールの使用に関する勧告やガイダンスを提供することで、臨床試験におけるAIやその他の技術の開発に積極的に取り組んでいます。
2024年11月、Bioforum (イスラエル)とメディデータ(フランス)は提携をさらに一歩進め、バイオテクノロジー分野のBioforum の顧客に対し、メディデータのAlベース技術へのアクセスを拡大しました。バイオフォーラムは Medidata Rave EDC と RTSM に加え、Medidata Clinical Data Studio と Medidata eConsent を採用し、臨床試験のデータ転送、品質、規制を強化します。
2024 年 4 月、IQVIA(米国)はセールスフォース(米国)と提携し、顧客エンゲージメントのためのライフサイエンスクラウド開発を加速。
2024年2月、Saama社(米国)はファイザー社(米国)と提携し、AIを活用してファイザー社のグローバルな臨床研究ポートフォリオ全体のデータレビュープロセスを合理化・迅速化するスマート・データ・クオリティ(SDQ)を拡大する複数年契約を締結。
2023年10月、Saama社(米国)はAstraZeneca社(英国)と、Saama社のAl-enabledテクノロジープラットフォームを使用して臨床データ管理とメディカルレビュープロセスを合理化するための複数年契約を締結しました。この契約は、スマート・データ・クオリティ(SDQ)、データハブ、ペイシェント・インサイト・ソリューションを組み込むことで、より迅速なデータロックとデータの効率的なレビューを促進し、医薬品開発のプロセスを早めることを目的としています。
臨床試験におけるAI市場の主要企業は以下の通りです。
IQVIA Inc. (US)
Saama. (US)
Dassault Systèmes (Medidata) (France)
Phesi (US)
PathAI, Inc. (US)
Unlearn.ai, Inc. (US)
Deep6.ai (US)
Microsoft (US)
IBM (US)
NVIDIA Corporation (US)
Insilico Medicine (US)
ConcertAI. (US)
AiCure. (US)
Median Technologies. (France)
Lantern Pharma Inc. (US)
Citeline, a Norstella Company (US)
Tempus AI, Inc. (US)
TriNetX, LLC (US)
ReviveMed Inc. (US)
Euretos. (US)
VeriSIM Life. (US)
Triomics (US)
Ardigen (Poland)
QuantHealth Ltd. US)
DEEP GENOMICS. (Canada)
【目次】
はじめに
1
研究方法論
15
要旨
27
プレミアムインサイト
56
市場概要
78
5.1 はじめに
5.2 市場ダイナミクス 市場促進要因 市場阻害要因 市場機会 市場課題
5.3 業界動向
5.4 エコシステム分析
5.5 ケーススタディ分析
5.6 バリューチェーン分析
5.7 ポーターの5つの力分析 供給者の交渉力 買い手の交渉力 代替品の脅威 新規参入の脅威 競争相手の強さ
5.8 規制分析 北米-ヨーロッパ-アジア太平洋-中南米-中東・アフリカ 規制機関、政府機関、その他の組織
5.9 特許分析 臨床試験におけるaiの特許公開動向 管轄地域と上位出願者分析
5.10 技術分析 主要技術-機械学習(ml)-自然言語処理(nlp)-コンピュータビジョン 補完技術-モノのインターネット(iot)-クラウドコンピューティング 隣接技術-先進ゲノミクス
5.11 業界動向
5.12 価格分析(定性) 主要オファリングの指標価格(2023年) 主要オファリングの指標価格(地域別)(2023年
5.13 主要会議・イベント(2024-2025年
5.14 主要ステークホルダーと購入基準 購入プロセスにおける主要ステークホルダー 購入基準
5.15 顧客のビジネスに影響を与えるトレンドと混乱
5.16 エンドユーザー分析 アンメットニーズ エンドユーザーの期待
5.17 臨床試験におけるAI市場:投資と資金調達シナリオ
5.18 臨床試験におけるAI市場:ビジネスモデル
5.19 臨床試験におけるAI市場へのAI/Gen AIの影響
臨床試験におけるAI市場:サービス別
97
6.1 導入
6.2 エンドツーエンドソリューション
6.3 ニッチソリューション
6.4 テクノロジープロバイダー
6.5 サービス コンサルティングサービス 導入サービス&継続的ITサポート トレーニング&教育サービス ポストセールス&メンテナンスサービス
臨床試験におけるAI市場、機能別
115
7.1 導入
7.2 患者のリクルート 患者の識別とスクリーニング 患者のエンゲージメントとリテンション サイトの最適化
7.3 治験デザイン最適化 ワークフロー管理 予測モデリング リスク管理
7.4 データ管理と品質管理
7.5 有害事象の予測と検出
7.6 薬剤の再利用
7.7 規制コンプライアンス
臨床試験におけるAI市場、フェーズ別
135
8.1 フェーズI
8.2 フェーズII
8.3 フェーズ III
8.4 第Ⅳ相
臨床試験におけるAI市場、展開モード別
148
9.1 導入
9.2 クラウドベースのソリューション パブリッククラウド プライベートクラウド マルチクラウド ハイブリッドクラウド
9.3 オンプレミス・ソリューション
臨床試験におけるAI市場:疾患別
155
10.1 はじめに
10.2 臨床検査
10.3 神経疾患
10.4 循環器疾患
10.5 代謝性疾患
10.6 感染症
10.7 免疫疾患
10.8 その他(消化器系、呼吸器系、生殖器系)
臨床試験におけるAI市場、技術別
167
11.1 導入
11.2 機械学習 深層学習 教師あり学習 教師なし学習 強化学習 その他のml技術(半教師あり学習、自己教師あり学習)
11.3 NLP
11.4 コンピュータビジョン
11.5 ロボティック・プロセス・オートメーション
11.6 その他
臨床試験におけるAI市場、用途別
170
12.1 導入
12.2 バイオマーカー
12.3 細胞・遺伝子治療
12.4 再生医療
12.5 医療機器・診断
臨床試験におけるAI市場、エンドユーザー別
172
13.1 導入
13.2 製薬・バイオテクノロジー企業
13.3 研究機関・研究所
13.4 医療機関
13.5 医薬品開発業務受託機関(CRO)
13.6 医療機器メーカー
…
【本レポートのお問い合わせ先】
www.marketreport.jp/contact
レポートコード:HIT 9229