
市場規模
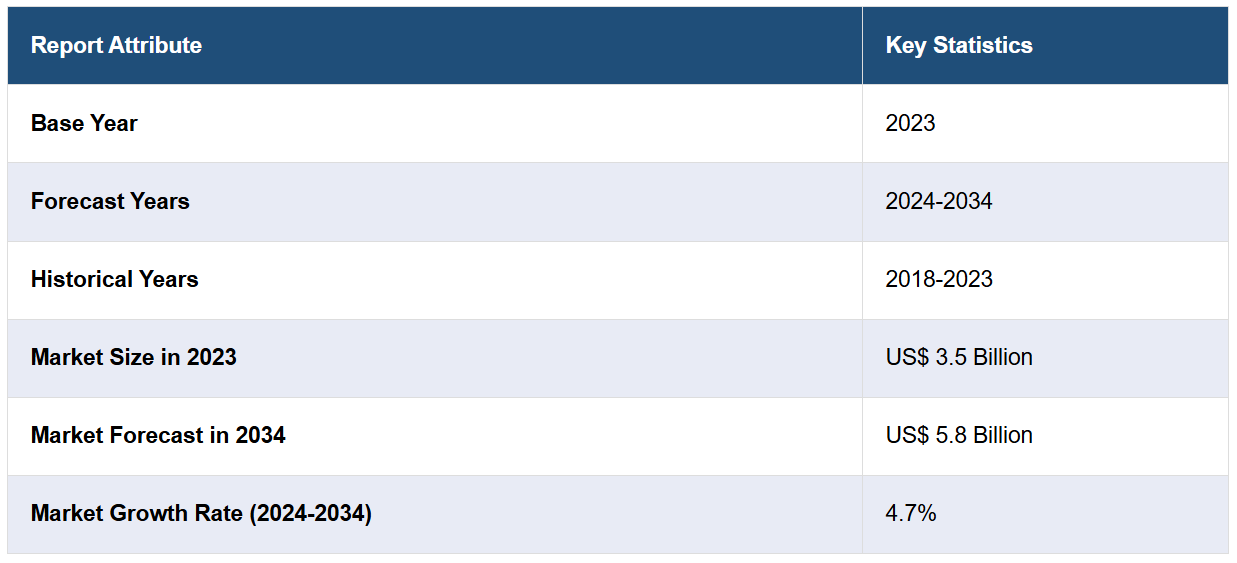
黄斑浮腫市場は、2023年のトップ7市場(米国、EU4か国、英国、日本)で35億米ドルの規模に達しました。今後、IMARC Groupは、2034年までにトップ7市場が58億米ドルに達し、2024年から2034年の年間平均成長率(CAGR)は4.7%になると予測しています。
黄斑浮腫市場は、IMARCの新しいレポート「黄斑浮腫市場:疫学、業界動向、シェア、規模、成長、機会、予測 2024年~2034年」で包括的に分析されている。黄斑浮腫は、鋭い視力や詳細な視力を司る網膜の中心部分である黄斑に体液が蓄積する状態を指す。この疾患により黄斑組織が腫れ、視界が歪んだりぼやけたりします。 症状は病気の重さによって異なりますが、中心視力の低下、白抜け、色覚の低下、読書や細かい作業が困難、視界の中心が暗くまたは空っぽに感じる、などがあります。 黄斑浮腫の診断は通常、患者の病歴や臨床症状の確認に加え、総合的な眼科検査を行います。医療従事者は、光干渉断層計(OCT)などの網膜画像技術を用いて黄斑の詳細な断面画像を取得し、液体の蓄積を視覚化して病気の重症度を評価することもあります。さらに、インドシアニングリーン蛍光眼底造影法やフルオレセイン蛍光眼底造影法を用いて、網膜血管の漏出や閉塞を観察することで診断を確定します。
高血糖レベルが網膜血管に損傷を与える糖尿病性網膜症の症例が増加していることが、黄斑浮腫市場を主に牽引しています。これに加えて、黄斑の正常な構造と機能を混乱させる可能性がある眼の外傷の増加も、市場に明るい見通しをもたらしています。さらに、この疾患の治療に抗血管内皮増殖因子の硝子体内注射が広く求められていることも、市場の成長をさらに後押ししています。これらの薬剤は、異常血管の発生を促進し、網膜の血管透過性を高める特定のタンパク質の作用を阻害し、黄斑部への体液の漏出を減少させます。これとは別に、レーザー治療の適用が拡大していることも、視力を安定させ、病状の進行を防ぐために網膜の患部に正確に制御されたエネルギーを照射するため、市場の成長を促すもう一つの重要な要因となっています。さらに、徐放性移植デバイスの人気が高まりつつあり、このデバイスは時間をかけてゆっくりと薬剤を放出することができ、患者の炎症を軽減できるため、予測期間中に黄斑浮腫市場を牽引することが期待されています。
IMARC Groupの最新レポートは、米国、EU4(ドイツ、スペイン、イタリア、フランス)、英国、日本の黄斑浮腫市場を徹底的に分析しています。これには、治療の実施状況、市場内、パイプラインの薬剤、個々の治療法のシェア、7つの主要市場にわたる市場実績、主要企業およびその薬剤の市場実績などが含まれます。また、本レポートでは、7つの主要市場にわたる現在の患者数と将来の患者数も提供しています。本レポートによると、黄斑浮腫の患者数が最も多いのは米国であり、その治療市場も最大です。さらに、現在の治療方法/アルゴリズム、市場の推進要因、課題、機会、償還シナリオ、未充足の医療ニーズなども報告書に記載されています。この報告書は、メーカー、投資家、事業戦略家、研究者、コンサルタント、そして黄斑浮腫市場に何らかの利害関係を有する方、または何らかの形で黄斑浮腫市場への参入を計画している方にとって必読の報告書です。
最近の動向:
2024年1月、協和キリンは、糖尿病黄斑浮腫の治療薬であるKHK4951(一般名:チボザニブ)の第Ⅱ相臨床試験を日本、北米、韓国、オーストラリアで開始した。協和発酵キリンは、糖尿病黄斑浮腫(DME)患者を対象としたチボザニブ点眼薬(KHK4951)の第2相臨床試験において、最初の患者登録が完了したと発表した。
2024年1月、EyePoint Pharmaceuticals, Inc.は、糖尿病黄斑浮腫(DME)を対象としたEYP-1901の第2相VERONA臨床試験において、最初の患者への投与が実施されたと発表しました。EYP-1901は、選択的チロシンキナーゼ阻害剤であるボロラニブを含む持続放出療法の試験薬です。
2023年11月、糖尿病合併症の治療に重点的に取り組むmRNA治療企業Exonate Ltd.は、同社の眼科領域の主力製品であるEXN407が、フェーズIB/IIA試験で事前に規定された評価項目を達成したと発表した。試験中、EXN407はすべての安全性および薬物動態パラメータを満たし、生物学的活性の有望な兆候を示した。
2023年10月、ロシュグループのジェネンテック社は、網膜静脈閉塞症(RVO)に伴う黄斑浮腫の治療薬であるVabysmo(faricimab-svoa)について、米国食品医薬品局(FDA)より承認を取得した。
2023年8月、レジェノロン・ファーマシューティカルズ社は、黄斑浮腫の治療薬であるアイリーア(アフリベルセプト)について、米国食品医薬品局(FDA)より承認を取得した。
2023年4月、中外製薬株式会社は、網膜静脈閉塞症に伴う黄斑浮腫の治療薬として、抗VEGF/抗Ang-2二特異性抗体Vabysmo硝子体内注射120mg/mLファリシムブ)について、厚生労働省に追加申請を行った。
主なハイライト:
黄斑浮腫の有病率は5.47%で、全体では低中所得国で5.81%、高所得国で5.14%でした。
Lundeenらは、黄斑浮腫の年間有病率が62%上昇していることを発見しました。さらに、女性と比較して男性の方が黄斑浮腫の有病率が高いことも観察されました。
黄斑浮腫(ME)の発生率は糖尿病の種類によって異なり、1型糖尿病では4.1%から7.9%、2型糖尿病では1.4%から12.8%となっています。
薬剤:
ルセンティス(ラニビズマブ)は硝子体内投与される薬剤で、血管内皮増殖因子(VEGF)阻害剤に分類されます。新生血管(ウェット型)加齢黄斑変性(AMD)、網膜静脈閉塞症(RVO)に伴う黄斑浮腫、糖尿病黄斑浮腫(DME)の治療薬として承認されています。このモノクローナル抗体フラグメントは、IgG1 kappaアイソタイプに属し、AMDの病態生理に関与する糖タンパク質であるヒト血管内皮増殖因子A(VEGF-A)を特異的に標的とします。2006年にFDA、2007年に欧州委員会(EC)で承認されたルセンティスには、バイオシミラーであるBYOOVIZという名称の製品があり、2022年3月にカナダ保健省(Health Canada)で承認されています。 その他のバイオシミラーであるCIMERLI、RAIVISIO、RANOPTOは、2022年8月にFDA、EC、カナダ保健省で承認されています。
Eylea(アフリベルセプト)は、ルセンティスと同様の適応症を持つ別のVEGF阻害剤であり、同様に硝子体内投与される。Eyleaは、新生血管黄斑変性、網膜静脈閉塞症関連黄斑浮腫、糖尿病黄斑浮腫に加え、未熟児網膜症および糖尿病性網膜症の治療薬として承認されている。FDAは2023年2月に未熟児網膜症、同年8月にその他の適応症に対してアイリーアを承認した。アフリベルセプトのバイオシミラーであるイェサフィリは、2023年9月にEUで承認された。
Vabysmoとして販売されているファリシマブは、AMDおよびDMEの治療を目的としてVEGF-AとAng-2の両方を標的とする二特異性抗体である。ルセンティスやアイリーアと同様に、硝子体内投与される。2022年1月にFDA、2022年5月にカナダで承認されたファリシマブは、細胞内異化作用により、より小さなペプチドやアミノ酸に分解された後、腎排泄される。
調査対象期間
ベース年:2023年
過去の期間:2018年~2023年
市場予測:2024年~2034年
対象国
米国
ドイツ
フランス
英国
イタリア
スペイン
日本
各国の分析内容
過去の、現在の、および将来の疫学シナリオ
過去の、現在の、および将来の黄斑浮腫市場の実績
市場における各種治療カテゴリーの過去の、現在の、および将来の実績
黄斑浮腫市場における各種薬剤の売上
市場における償還シナリオ
市場内および開発中の薬剤
競合状況
このレポートでは、現在の黄斑浮腫治療薬と後期開発段階にある薬剤の詳しい分析も提供しています。
市場で販売されている薬剤
薬剤概要
作用機序
規制状況
臨床試験結果
薬剤の普及状況と市場実績
後期開発段階にある薬剤
薬剤概要
作用機序
規制状況
臨床試験結果
薬剤の普及状況と市場実績
【目次】
1 序文
2 範囲と方法論
2.1 本調査の目的
2.2 利害関係者
2.3 データソース
2.3.1 一次ソース
2.3.2 二次ソース
2.4 市場推定
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測方法論
3 エグゼクティブサマリー
4 黄斑浮腫 – イントロダクション
4.1 概要
4.2 規制プロセス
4.3 疫学(2018~2023年)および予測(2024~2034年
4.4 市場概要(2018~2023年)および予測(2024~2034年
4.5 競合情報
5 黄斑浮腫 – 疾患概要
5.1 はじめに
5.2 症状と診断
5.3 病態生理学
5.4 原因とリスク要因
5.5 治療
6 患者の経過
7 黄斑浮腫 – 疫学と患者数
7.1 疫学 – 主要な洞察
7.2 疫学シナリオ – トップ7市場
7.2.1 疫学シナリオ(2018年~2023年
7.2.2 疫学予測(2024年~2034年)
7.2.3 年齢別疫学(2018年~2034年)
7.2.4 性別疫学(2018年~2034年)
7.2.5 診断例(2018年~2034年)
7.2.6 患者数/治療例(2018年~2034年)
7.3 疫学シナリオ – 米国
7.3.1 疫学シナリオ(2018年~2023年)
7.3.2 疫学予測(2024年~2034年)
7.3.3 年齢別疫学(2018年~2034年)
7.3.4 性別による疫学(2018年~2034年)
7.3.5 診断された症例(2018年~2034年)
7.3.6 患者数/治療された症例(2018年~2034年)
7.4 疫学シナリオ – ドイツ
7.4.1 疫学シナリオ(2018年~2023年)
7.4.2 疫学予測(2024年~2034年)
7.4.3 年齢別疫学(2018年~2034年)
7.4.4 性別疫学(2018年~2034年)
7.4.5 診断例(2018年~2034年)
7.4.6 患者数/治療例数(2018年~2034年)
7.5 疫学シナリオ – フランス
7.5.1 疫学シナリオ(2018年~2023年)
7.5.2 疫学予測(2024年~2034年)
7.5.3 年齢別疫学(2018年~2034年)
7.5.4 性別による疫学(2018年~2034年)
7.5.5 診断された症例(2018年~2034年)
7.5.6 患者数/治療された症例(2018年~2034年)
7.6 英国の疫学シナリオ
7.6.1 疫学シナリオ(2018年~2023年)
7.6.2 疫学予測(2024年~2034年)
7.6.3 年齢別疫学(2018年~2034年)
7.6.4 性別疫学(2018年~2034年)
7.6.5 診断例(2018年~2034年)
7.6.6 患者数/治療例(2018年~2034年)
7.7 疫学シナリオ – イタリア
7.7.1 疫学シナリオ(2018年~2023年)
7.7.2 疫学予測(2024年~2034年)
7.7.3 年齢別疫学(2018年~2034年)
7.7.4 性別による疫学(2018~2034年)
7.7.5 診断された症例(2018~2034年)
7.7.6 患者数/治療された症例(2018~2034年)
7.8 疫学シナリオ – スペイン
7.8.1 疫学シナリオ(2018~2023年)
7.8.2 疫学予測(2024年~2034年)
7.8.3 年齢別疫学(2018年~2034年)
7.8.4 性別疫学(2018年~2034年)
7.8.5 診断された症例(2018年~2034年)
7.8.6 患者数/治療例数(2018年~2034年)
7.9 日本の疫学シナリオ
7.9.1 疫学シナリオ(2018年~2023年)
7.9.2 疫学予測(2024年~2034年)
7.9.3 年齢別疫学(2018年~2034年)
7.9.4 性別ごとの疫学(2018年~2034年)
7.9.5 診断された症例(2018年~2034年)
7.9.6 患者数/治療された症例(2018年~2034年)
8 黄斑浮腫 – 治療アルゴリズム、ガイドライン、医療行為
8.1 ガイドライン、管理、治療
8.2 治療アルゴリズム
9 黄斑浮腫 – 未充足ニーズ
10 黄斑浮腫 – 治療の主要評価項目
11 黄斑浮腫 – 上市製品
11.1 トップ7市場における黄斑浮腫の上市薬剤一覧
11.1.1 ルセンティス(ラニビズマブ) – ジェネンテック/ノバルティス・ファーマシューティカルズ
11.1.1.1 薬剤概要
11.1.1.2 作用機序
11.1.1.3 規制当局による審査状況
11.1.1.4 臨床試験結果
11.1.1.5 主要市場での売上
11.1.2 Eylea(アフリベルセプト) – バイエル/レジェネロン・ファーマシューティカルズ/サノフィ
11.1.2.1 製品概要
11.1.2.2 作用機序
11.1.2.3 規制状況
11.1.2.4 臨床試験結果
11.1.2.5 主要市場での売上
11.1.3 オズデックス(デキサメタゾン点眼薬) – AbbVie
11.1.3.1 製品概要
11.1.3.2 作用機序
11.1.3.3 規制状況
11.1.3.4 臨床試験結果
11.1.3.5 主要市場での売上
…
【お問い合わせ・ご購入サイト】
資料コード:SR112025A8127
